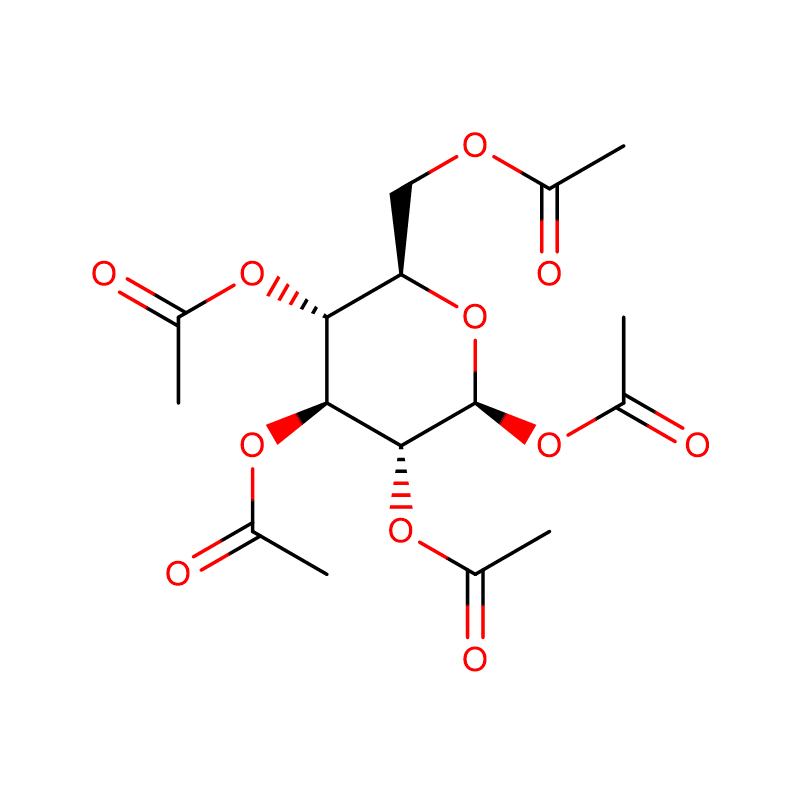
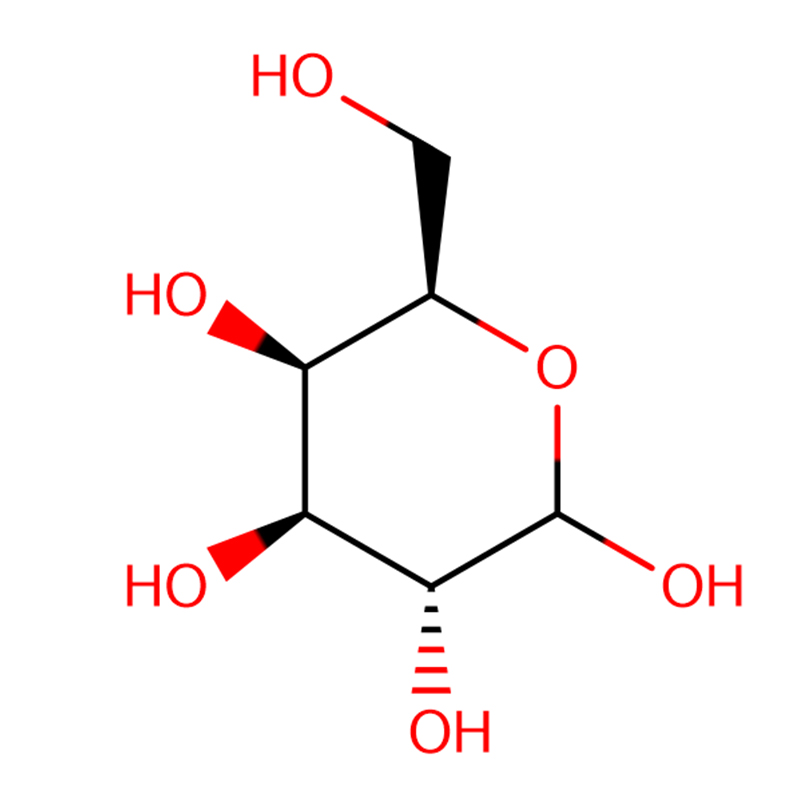
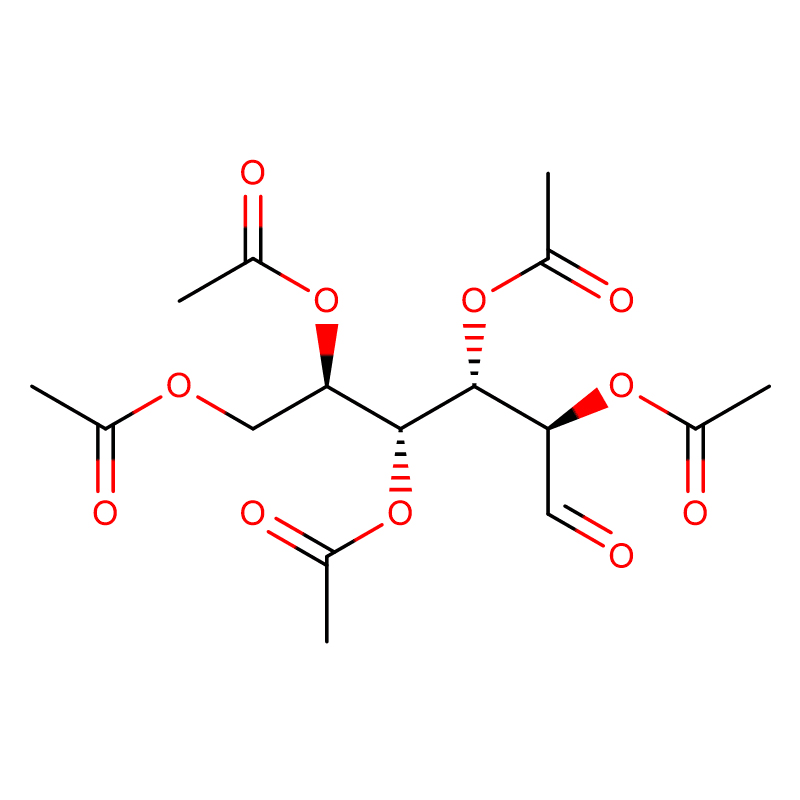
4-NITROFENYLI-ALFA-D-MANNOPYRANOSIDI CAS:10357-27-4 Luonnonvalkoinen jauhe 98 %
| Luettelonumero | XD90011 |
| tuotteen nimi | 4-nitrofenyyli-alfa-D-mannopyranosidi |
| CAS | 10357-27-4 |
| Molekyylikaava | C12H15NO8 |
| Molekyylipaino | 30301.25 |
| Tallennustiedot | -2-8°C |
| Yhdenmukaistettu tariffikoodi | 29400000 |
Tuotteen tiedot
| Vesi | <5% Karl Fische |
| Liukoisuus | 1 % DMF:ssä on kirkasta ja väritöntä |
| Puhtaus | Vapaa 4-nitrofenoli <200 ppm |
| HPLC | >98 % |
| Ulkomuoto | Luonnonvalkoinen jauhe |
Mekanistisia näkemyksiä Ca2+-riippuvaisesta alfa-mannosidaasien perheestä ihmisen suoliston symbiontissa.
Paksusuolen bakteereilla, joista esimerkkinä on Bacteroides thetaiotaomicron, on keskeinen rooli ihmisten terveyden ylläpitämisessä valjastamalla suuria glykosidihydrolaasien perheitä (GH) hyödyntämään ravinnon polysakkarideja ja isäntäglykaaneja ravintoaineina.Tällaisesta GH-perheen laajenemisesta on esimerkkinä B. thetaiotaomicronin genomin koodaamat 23 perheen GH92-glykosidaasit.Tässä osoitamme, että nämä ovat alfa-mannosidaaseja, jotka toimivat yhden syrjäytysmekanismin kautta hyödyntäen isännän N-glykaaneja.Kahden GH92-mannosidaasin kolmiulotteinen rakenne määrittelee kahden domeenin proteiinien perheen, jossa katalyyttinen keskus sijaitsee domeenin rajapinnassa tarjoten happoa (glutamaattia) ja emästä (aspartaattia) apua hydrolyysille Ca(2+)- riippuvaisella tavalla.GH92:n kolmiulotteiset rakenteet kompleksina estäjien kanssa antavat käsityksen katalyysin spesifisyydestä, mekanismista ja konformaatioreitistä.Ca(2+):lla on keskeinen katalyyttinen rooli auttaessaan vääristämään mannosidia pois sen perustilasta (4)C(1) -tuolin konformaatiosta kohti siirtymätilaa. (Bibliografia: Nat.Chem.Biol.6, 125-32, (2010)
Ovalbumiiniglykoasparagiinien frontaalinen affiniteettikromatografia concanavalin A-Sepharose -pylväässä.Kvantitatiivinen tutkimus lektiinin sitoutumisspesifisyydestä.
Sepharose 4B:llä immobilisoidun konkanavaliini A:n (ConA) vuorovaikutuksia 10 ovalbumiinista peräisin olevan glykoasparagiinin kanssa tutkittiin kvantitatiivisesti frontaaliaffiniteettikromatografialla.Tässä menetelmässä hiilihydraattiliuosta levitetään jatkuvasti ConA-Sepharose-kolonniin ja eluutiorintaman hidastuminen mitataan vuorovaikutuksen voimakkuuden parametrina.Dissosiaatiovakio (Kd) kullekin sakkaridille ConA:n kanssa voidaan määrittää.Analyysi p-nitrofenyyli-alfa,D-mannosidin sitoutumisesta on osoittanut, että ConA:n sitoutumisominaisuudet eivät muutu olennaisesti Sepharose 4B:lle immobilisoinnin jälkeen.Jokainen ovalbumiiniglykoasparagiineista leimattiin tritiumilla pelkistävällä metylaatiomenetelmällä analysointia varten.Saatujen Kd-arvojen vertailu osoitti, että ConA:n sitoutuminen vaihtelee huomattavasti glykosyyliketjun hyvin pienillä rakenteellisilla eroilla.Tulokset viittaavat siihen, että ConA tunnistaa spesifisen glykosyyliketjurakenteen, Man alfa 1-6(Man alfa 1-3)Man, jossa vähintään yhden hydroksyyliryhmän C-6-kytketyn mannoosin C-3-asemassa pitäisi olla vapaa.